- De déterminer la longueur d'onde absorbée par une solution : en éclairant la solution graduellement de l'ultra-violet a l'infra-rouge, il sera aisé de déterminer la longueur d'onde absorbée par la solution en observant la chute du signal (diminution de la lumière réfléchie, tout comme la pomme, à la longueur d'onde absorbée la solution semble "noire"). C'est ce que l'on appelle la couleur complémentaire
- L'absorbance d'une solution étant directement liée à sa concentration (dans notre exemple, plus le rouge de la pomme est intense, plus elle nous paraîtra noire lorsqu'éclairée avec une lumière bleue-verte, à l'inverse elle nous paraîtra grise si sa couleur est d'un rouge plus pâle), un spectrophotomètre permet de déterminer la concentration d'une solution si on connaît sa longueur d'onde absorbée.
Cette relation a été décrite en parti par les physiciens Pierre Bouguer (1729) et Jean-Henri Lambert (1760), puis complétée avec la relation de proportionnalité entre l'absorbance et la concentration d'une substance en solution par August Beer (1852) : c'est la loi de Beer-Lambert-Bouguer.
SECONDAIRE | DIFFICULTÉ DIFFICILE | 4 À 6 HEURES
Résumé de l'activité
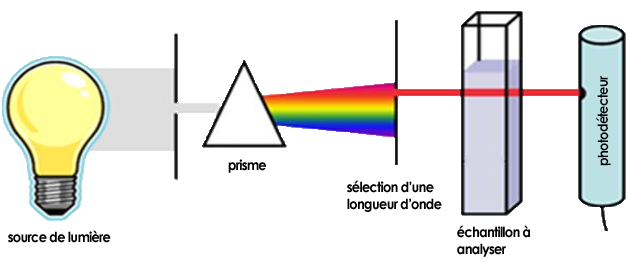
Objectif
- Déterminer les longueurs d'ondes absorbées par différents colorants (couleur complémentaire à la substance colorée).
- Vérifier la correspondance entre concentration et absorbance d'une solution, à une longueur d'onde donnée. Nous n'allons pas doser précisément la concentration d'une solution par spectrophotométrie, mais tout du moins tracer une courbe étalon qui nous permettrait de le faire.
Étape par étape, nous allons :
- Étape 1 : Mettre en place le système expérimental : montage électronique et programmation.
- Étape 2 : Determiner les longueurs d'onde absorbées par différents colorants : rouge, vert et bleu.
- Étape 3 : Vérifier la relation de proportionalité entre absorbance et concentration d'une solution de bleu de méthylène : la loi de Beer-Lamber-Bouguer.
Bon travail !
Matériel
- Arduino UNO/Genuino.
- DEL RGB (Red, Green, Blue): ici nous utilisons une DEL RGB Keyes, modèle KY-016 voir ici.
- Photorésistance : ici nous utilisons une photorésistance Keyes, modèle KY-018, voir ici.
- Fils et breadboard.
- Cuve de spectrophotométrie en plastique ou tout autre contenant transparent de 1 à 1,5 cm de diamètre ou de largeur.
- Un porte cuve que vous pourrez fabriquer vous même en carton noir, ou pour les plus chanceux imprimer en 3D.
- Colorants alimentaires ou de laboratoire bleu, vert et rouge.
- Eau distillée (à la maison de l'eau du robinet pourra faire l'affaire).
Il est maintenant très aisé de designer soit même ses objets 3D. Le site web Tinkercad est très bien fait pour ça, et extrèmement facile d'approche. Les utilisateurs de Windows 10 auront également le logiciel Windows 3D Builder qui est très facile d'utilisation.
Bien que je vous encourage fortement à dessiner vous même votre porte cuve (avec 2 orifices en vis à vis pour la DEL et la photoresistance), les plus fénéants pourront télécharger le fichier 3D pour imprimer le porte cuve au format obj ou stl.
Mise en place du protocole expérimental
Montage electronique
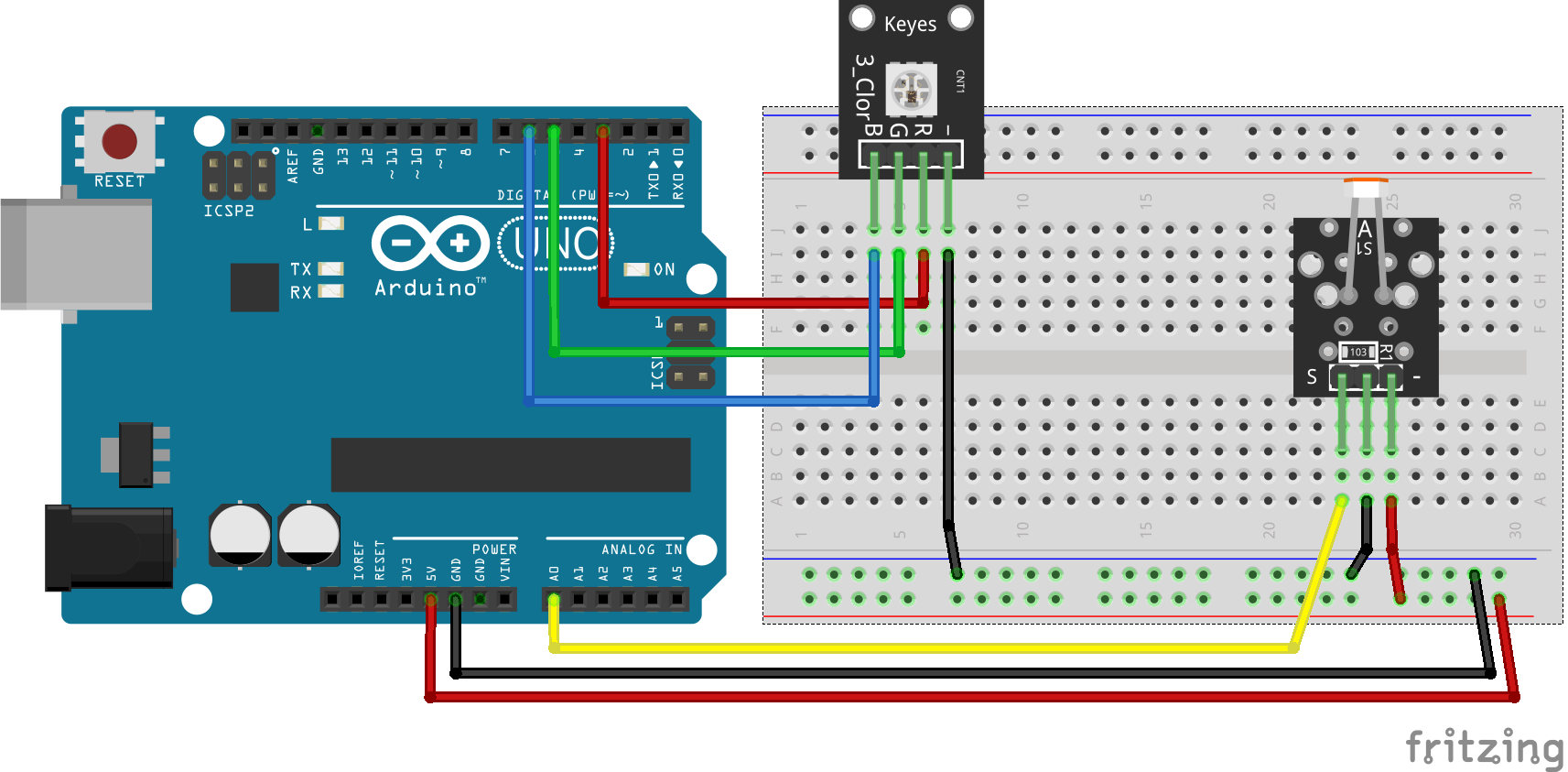
- La DEL RGB est branchée sur les pin 3 (pin "R" - rouge), 5 (pin "G" - vert) et 6 (pin "B" - bleu) de l'Arduino (pin PWM).
- La photorésistance (pin "S" - signal) est branchée sur la pin A0 (analogique).
NOTE : vous constaterez que la photorésistance est branchée à l'envers : la pin "-" sur le 5V et la pin "+" sur le Ground. En effet, le composant est fait pour être résistif avec la lumière. Plus la lumière augmente, plus la photorésistance sera "résistante" et plus le signal sera faible. Intuitivement, nous voulons que l'intensité lumineuse et le signal aux bornes de la photorésistance soient directement proportionnels. Le petit truc consite donc à inverser le signal en la branchant à l'envers. Nous aurions aussi pu faire un petit tour de passe-passe mathématique dans le code...
Un peu de code...
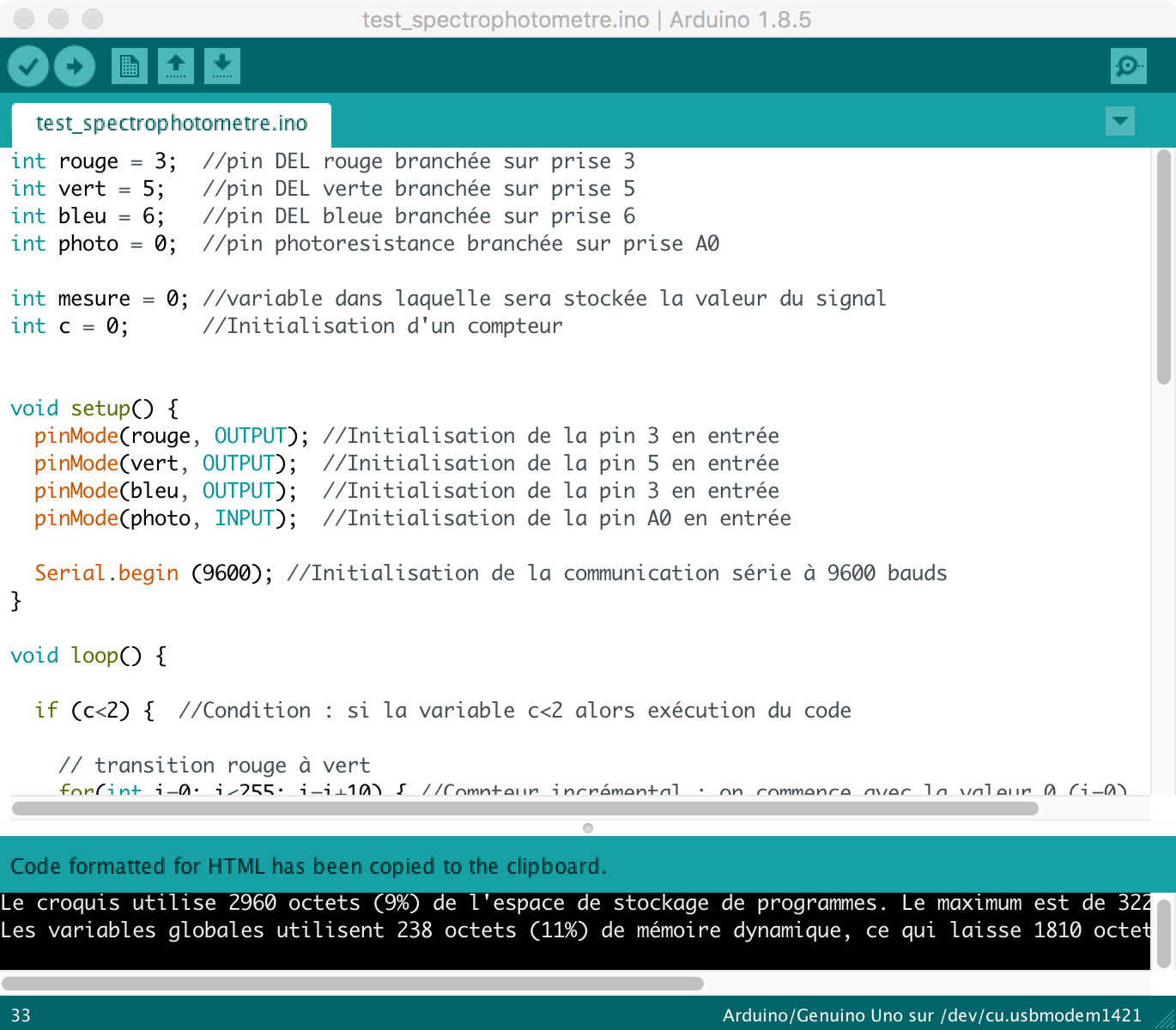
Faire un fading de couleur avec une DEL RGB n'est pas si facile si on ne veut pas sombrer dans les tableaux qui sont une notion un peu complexe pour ce travail pratique. Nous allons utiliser les boucles incrémentielles "for" pour parvenir à nos fins. Tapons le code et attardons-nous à le comprendre ligne par ligne !
int rouge = 3; //pin DEL rouge branchée sur prise 3
int vert = 5; //pin DEL verte branchée sur prise 5
int bleu = 6; //pin DEL bleue branchée sur prise 6
int photo = 0; //pin photoresistance branchée sur prise A0
int mesure = 0; //variable dans laquelle sera stockée la valeur du signal
int c = 0; //Initialisation d'un compteur
void setup() {
pinMode(rouge, OUTPUT); //Initialisation de la pin 3 en entrée
pinMode(vert, OUTPUT); //Initialisation de la pin 5 en entrée
pinMode(bleu, OUTPUT); //Initialisation de la pin 3 en entrée
pinMode(photo, INPUT); //Initialisation de la pin A0 en entrée
Serial.begin (9600); //Initialisation de la communication série à 9600 bauds
}
void loop() {
if (c<2) { //Condition : si la variable c<2 alors exécution du code
// transition rouge à vert
for(int i=0; i<255; i=i+10) { //Compteur incrémental : on commence avec la valeur 0 (i=0),
//on fini avec la valeur 254 (i<255),
//on incrémente de 10 à chaque boucle (i=i+10)
analogWrite(rouge, 255-i); //On commence avec la pin rouge allumée
//(valeur PWM 255-i avec i=0 initialement - voir "for")
//puis on la diminue de 10 à chaque boucle (255-(i+10) à chaque boucle)
analogWrite(vert, i); //La pin verte commence éteine (i=0)
//puis on l'augmente de 10 à chaque boucle (i=i+10)
analogWrite(bleu, 0); //La pin bleue reste pour le moment éteinte
mesure = analogRead (photo); //On effectue une mesure aux bornes de la photoresistance
Serial.print ("rouge - vert , "); //On affiche dans le moniteur série la chaine de caractère
Serial.println (mesure); //On affiche dans le moniteur série la valeur mesurée
delay(300); //Pause de 300ms entre les boucles
}
// transition vert à bleu - même démarche que précédemment
for(int i=0; i<255; i=i+10) {
analogWrite(vert, 255-i);
analogWrite(bleu, i);
analogWrite(rouge, 0);
mesure = analogRead (photo);
Serial.print ("vert - bleu , ");
Serial.println (mesure);
delay(300);
}
// transistion bleu à rouge - même démarche que précédemment
for(int i=0; i<255; i=i+10) {
analogWrite(bleu, 255-i);
analogWrite(rouge, i);
analogWrite(vert, 0);
mesure = analogRead (photo);
Serial.print ("bleu - rouge , ");
Serial.println (mesure);
delay(300);
}
c++; //La valeur du compteur est incrémentée de 1 suite à l'éxécution de cette partie de programme
}
}
Dans un premier temps nous déclarons les variables.
- Déclaration des noms de pin avec leurs numéros associés (exemple : "int rouge = 3;" signifiant que la chaine de caractère "rouge" devra être interprétée comme la valeur numérique "3").
- Déclaration de la variable "mesure" qui nous permettra de stocker le signal lu par la photorésitance.
- Déclaration de la variable "c" qui nous permettra de mettre en place un compteur de boucle et d'arreter le programme en tant voulu (il y aura déjà 75 valeurs recueillies par boucle, imaginez si vous laisser tourner votre programme durant 10 ou 20 boucles !).
Puis vient la partie d'initialiation : le void setup
Très simple, pas de surprises :- Déclaration des pin "rouge", "vert", "bleu" et "photo" en entrée ou en sortie.
- Initialisation de la communication série à 9600 bauds qui nous permettra d'afficher le signal lu par la photorésistance, dans le moniteur série.
Et pour finir, la boucle principale : le void loop.
Quatre sections importantes:-
- if.
- for 1 (transition rouge à vert).
- for 2 (transition vert à bleu).
- for 3 (transition bleu à rouge).
- Éxecution conditionnelle du programme (if).
- La condition qui doit obligatoirement êre remplie pour permettre l'éxecution du bout de programme compris entre les deux accolades du if est indiquée entre parenthèse : c < 2. Nous y reviendrons un peu plus tard.
- Le compteur est incrémenté de +1 (c++) à la toute fin du programme.
Ainsi, à chaque fois que la condition c < 2 est remplie, l'Arduino exécute la partie de programme comprise entre les 2 accolades du if. A chaque fois qu'il exécute cette partie de programme, la valeur de la variable c augmente de 1. Lorsque la variable c sera égale à 2, la condition ne pourra plus être remplie et le programme s'arrêtera.
Le programme va donc éxécuter 2 fois la condition.
NOTE : Pourquoi 2 fois ? Si par exemple notre substance absorbe le rouge pur, ce sera la première valeur du tableau. Comment savoir que ce n'est pas un artefact ? Souvent au démarrage du programme, la toute première valeur est aberrante : latence, interférence, c'est un phénomène que l'on obeserve souvent. Donc pour être surs de la validité de nos données, nous repassons tout le spectre lumineux 2 fois. Cela nous permettra également de vérifier, en une seule exécution, la reproductibilité des résultats.
- La boucle
incrémentielle (for).
Elle permet d'incrémenter une variable à chaque boucle exécutée par le programme.
Elle est formatée de la manière suivante :
for (variable à incrémenter et sa valeur de départ; valeur maximale que doit prendre la variable - la boucle for s'arretera lorsque la variable sera égale à cette valeur; incrément de la variable à chaque boucle).
Ici nous avons for (i=0; i < 255; i=i+10).
Nous utilisons une variable i dont la valeur de départ est 0, la boucle for devra être éxécutée jusqu'à ce que i soit strictement inférieur à 255, et la variable i sera additionnée (incrémentée) de 10 à chaque boucle d'éxécution du programme.- La pin rouge est tout d'abord allumée (analogWrite (rouge, 255-i) avec i initialement déclarée dans le for i = 0) et son intensité va diminuer à chaque boucle d'éxécution (en ayant déclaré l'incrément i = i+10 dans la boucle for : boucle for numéro 2 : i = 255-10, boucle for numéro 3 : i = 245-10, boucle for numéro 4 : i = 235-10 etc).
- De la même manière, la pin vert est tout d'abord éteinte (analogWrite (vert, i) avec i initialement déclarée dans le for i = 0)et son intensité va augmenter à chaque boucle d'éxécution (en ayant déclaré l'incrément i = i+10 dans la boucle for : boucle for numéro 2 : i = 10, boucle for numéro 3 : i = 20, boucle for numéro 4 : i = 30 etc).
- La pin bleu reste pour le moment éteine (analogWrite (bleu, 0)).
- Le signal lu par la photorésistance est stocké dans la variable mesure.
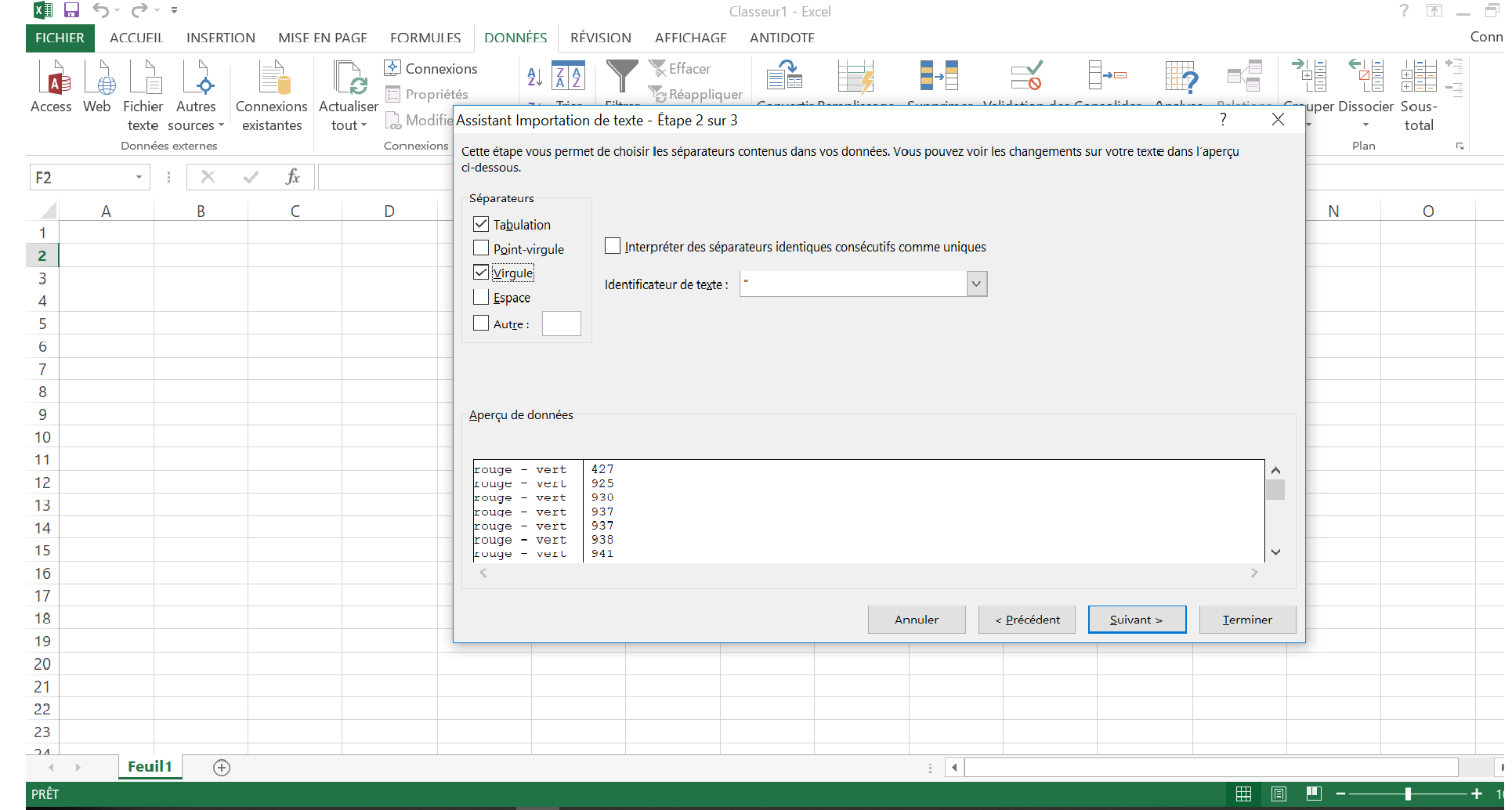
- La chaine de caractère (exemple "bleu-rouge") et le signal receuilli par la photorésistance seront affichés dans le moniteur série, espacés par une virgule (fonctions Serial.print et Serial.println pour le retour à la ligne).
Les données seront donc formatées de la manière suivante : couleur - couleur , mesure.
Ce format nous permettra de séparer et trier facilement nos données dans Excel, nous y viendrons plus tard. - Le programme est mis en pause durant 300 millisecondes (delay(300).
C'est cette ligne de code qui donne l'instruction d'effectuer un relevé toutes les 300 millisecondes.
A ce moment-ci, au fur et à mesure que l'intensité de rouge diminue, l'intensité de vert augmente. La DEL semblera donc prendre toutes les teintes du rouge au vert.
Les 2 autres boucles for fonctionnent sur le même principe, et permettent la transition du vert au bleu et du bleu au rouge.
Vous pouvez maintenant brancher votre Arduino et téléverser le programme.
Cliquez sur la loupe en haut à droite de la fenêre Arduino pour faire apparaître le moniteur série. Par défaut il sera réglé sur le débit de 9600 bauds.
Vous verrez alors dans la nouvelle fenêtre un message formaté de la manière suivante :
couleur-couleur , mesure.
Mise en place de l'expérience
La DEL RGB et la photorésistance doivent être parfaitement alignées pour une mesure optimale.
Bien sur, les mesures doivent avoir lieu dans un environnement sans lumière parasite : fabriquez votre porte cuve dans un carton épais noir, ou imprimez-le avec un plastique noir.
Aménagez 2 trous de 5 mm de diamètre parfaitement en vis-à-vis, dont le centre se situe à environ 8 mm du fond du porte cuve. Ces trous serviront à insérer la DEL RGB et la phtorésistance.
N'hésitez pas à télécharger le fichier 3D pour mieux visualiser le porte cuve (cliquez sur l'image ci-dessous).
Étapes expérimentales
- Préparez la solution colorée à étudier.
- Pipetez 1 mL de cette solution dans la cuve.
- Insérez la cuve dans le porte cuve.
- Démarrez le moniteur série.
- Attendez la fin de l'exécution du programme.
- Suivez les étapes ci-dessous pour importer vos données dans Excel (section "Analyse des résultats".
Analyse des résultats
Étude de l'absorbance du colorant vert
Voilà, vous êtes maintenant face à 75 lignes de chiffres dans le moniteur série du logiciel Arduino !
Mais que, quoi, comment faire ? Procédons par étapes :
- Commencez par sélectionner toutes les valeurs puis copiez-collez les dans votre éditeur de texte favori ("bloc-note" sous windows, "textedit" sous OSX).
Utilisez les raccourcis clavier :- Tout sélectionner : control + a (Windows) / cmd + a (OSX)
- Copier : control + c (Windows) / cmd + c (OSX)
- Coller dans votre éditeur de texte : control + v (Windows) / cmd + v (OSX)
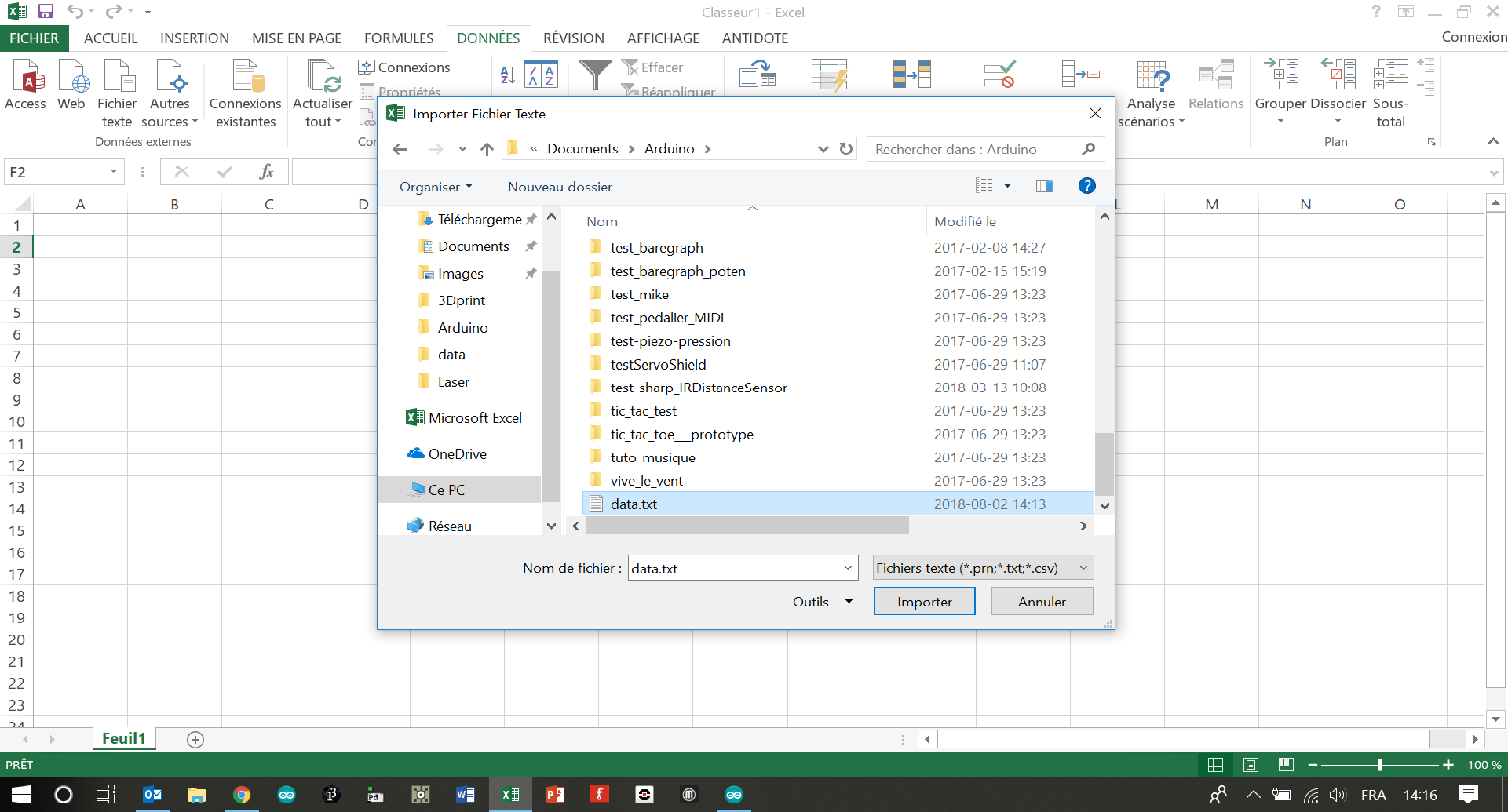
- Enregistrez votre document au format .txt (exemple : data.txt).
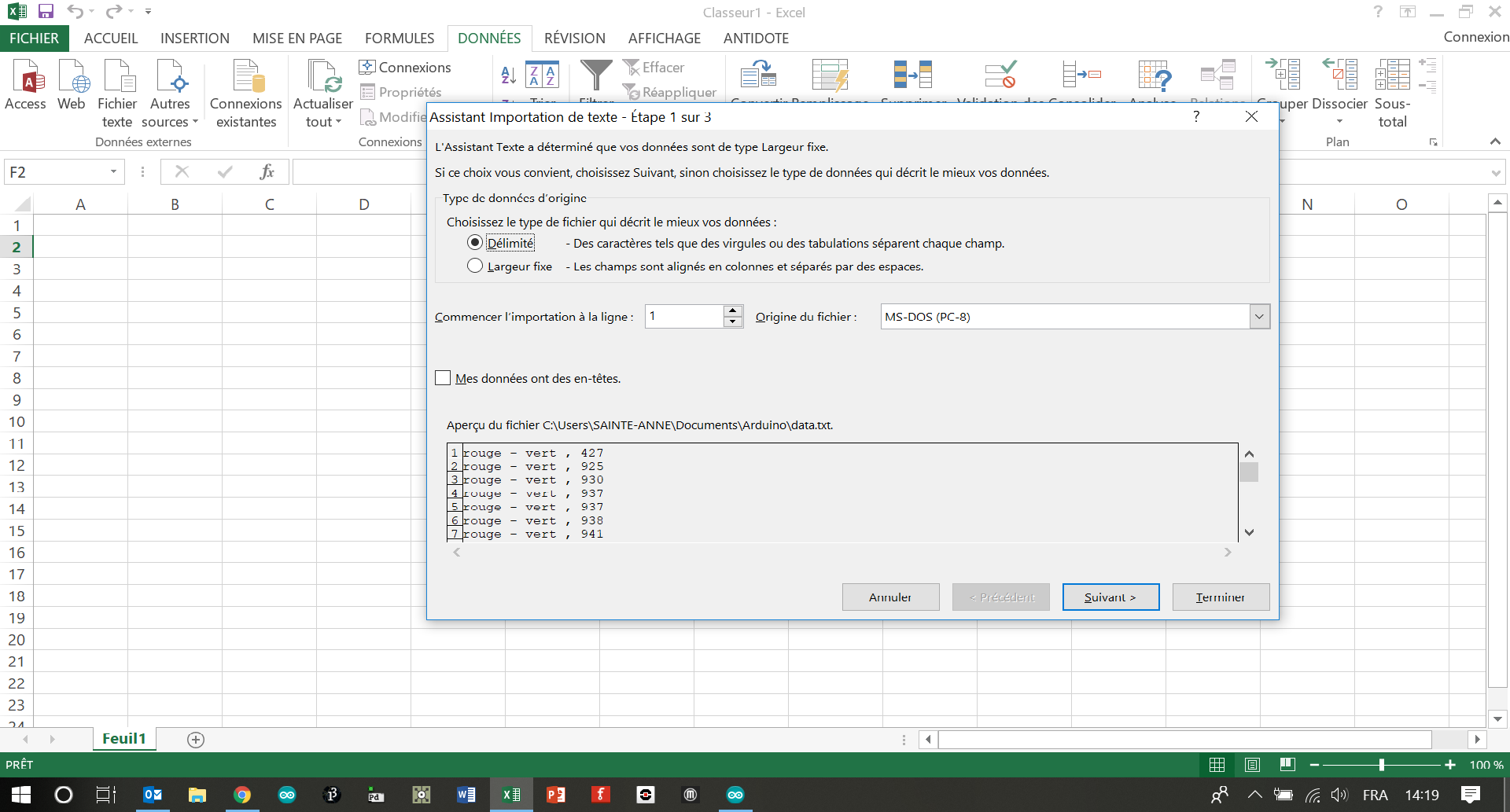
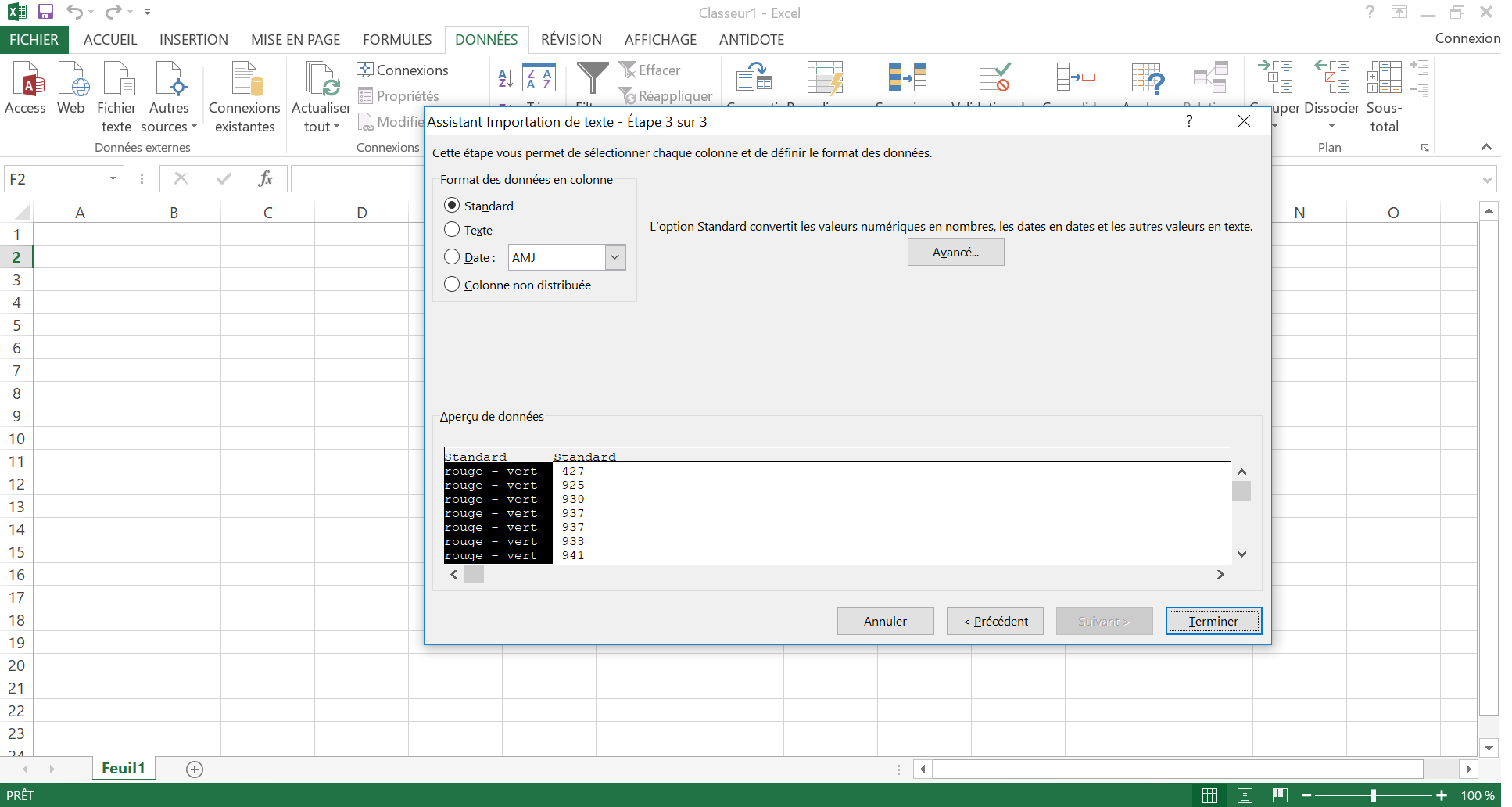
- Ouvrez votre tableur favori et créez un nouveau document. Je vais prendre le cas d'Excel pour la suite (cliquez sur les images pour les agrandir).
Vos données apparaisent maintenant sous forme de 2 colonnes dans Excel.
Insérez un graphique afin de représenter vos données : choisissez graphique en courbe.
Si vous avez bien travaillé, vous devriez obtenir un superbe spectrophotogramme montrant le pic d'absorption du colorant vert comme ceci :
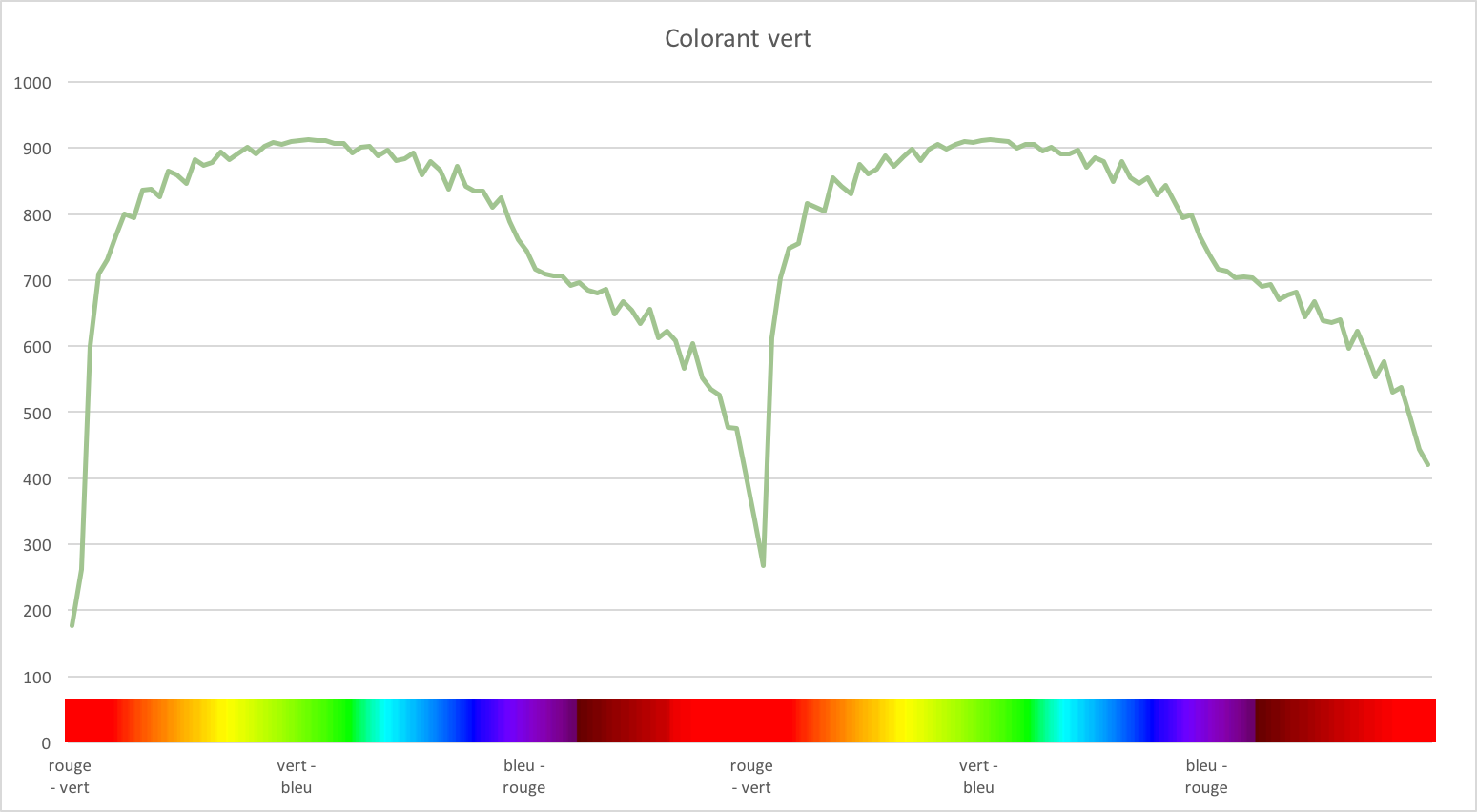
Comme vous pouvez voir dans le graphique, j'ai ajouté en abcisses un spectre de lumière visible correspondant à peu près aux couleurs émises par la DEL.
Vous pouvez le télécharger ici
Votre défi : adaptez le programme pour que le "fading" de couleurs correspondent à l'ordre du spectre !
Nous pouvons constater que le colorant vert absorbe légèrement dans le mauve puis de plus en plus dans le rouge. Les couleurs complémentraires au vert seraient donc le mauve et le rouge.
Voici un cercle chromatique. Il indique, pour chaque couleur, sa couleur complémentaire. Pour le lire, il suffit de regarder les couleurs qui sont l'une en face de l'autre. En face du vert figure les couleurs orange et rouge, nous pouvons valider que les couleurs complémentaires au vert sont bien l'orange et le rouge. La substance colorée verte absorbe donc la lumière rouge-orangée.
Afin de valider la pertinence des résultats obtenus avec notre petit montage Arduino, j'ai également mesuré l'absorbance de la même solution avec un spectrophotomètre Vernier professionnel.
Les résultats coïncident parfaitement ! Il y a 2 pics d'absorbance : un dans le mauve et un autre plus important dans le rouge orangé. Étant donné que notre spectre est à l'envers la courbe n'a pas la même allure, mais les résultats sont identiques.
Étudions maintenant la couleur complémentaire au bleu.
Étude de l'absorbance du colorant bleu
La démarche expérimentale est la même qu'à l'étape précédente :
- Préparez votre solution de colorant bleu.
- Pipetez 1 mL de cette solution dans une cuve propre.
- Insérez la cuve dans le porte cuve.
- Ouvrez le moniteur série et attendez que le programme s'éxécute.
- Copiez-collez le contenu du moniteur série dans un fichier .txt.
- Importez vos données à partir du fichier .txt dans Excel.
- Représentez vos données sous forme de graphique en courbe.
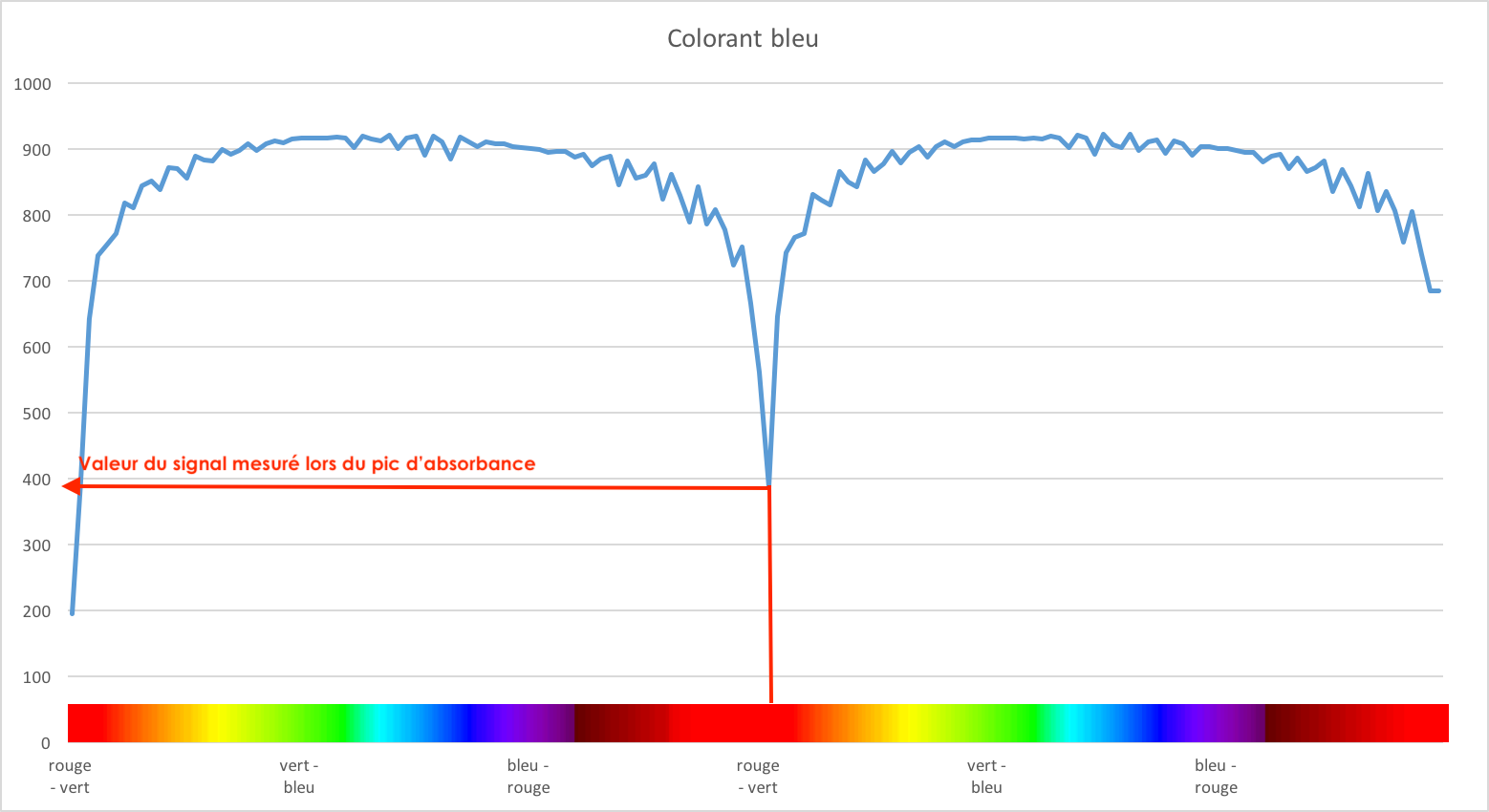
Mes résultats ressemblent à ceci, mais les vôtres peuvent être légèrement différents. En effet, vous avez maintenant compris qu'en fonction de la teinte de votre colorant la couleur absorbée peut être différente.
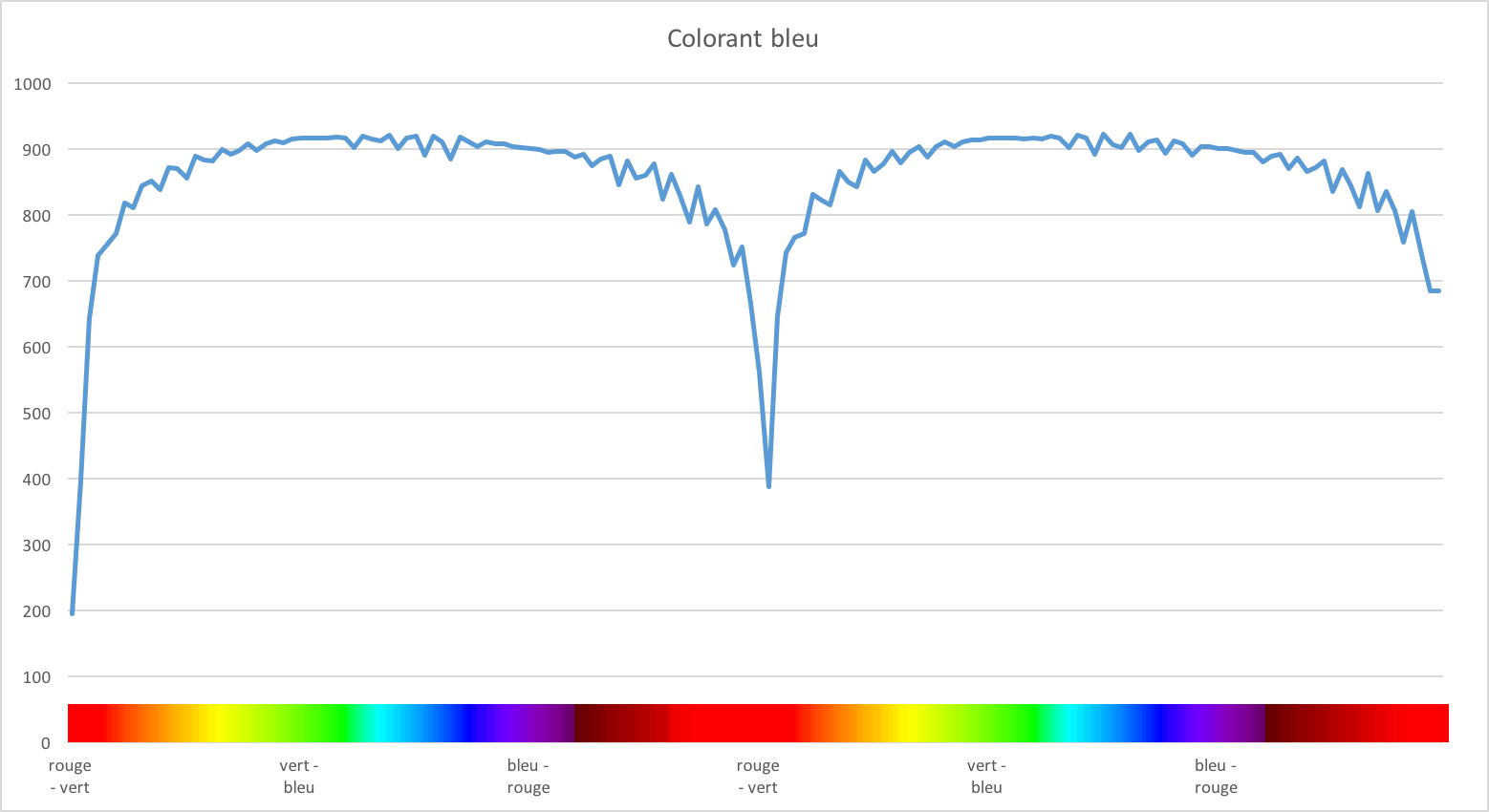
Nous observons un pic bien distinct dans le rouge-orangé. Si l'on se réfère au cercle chromatique, le bleu pâle absorbe en effet dans cette gamme de couleur.
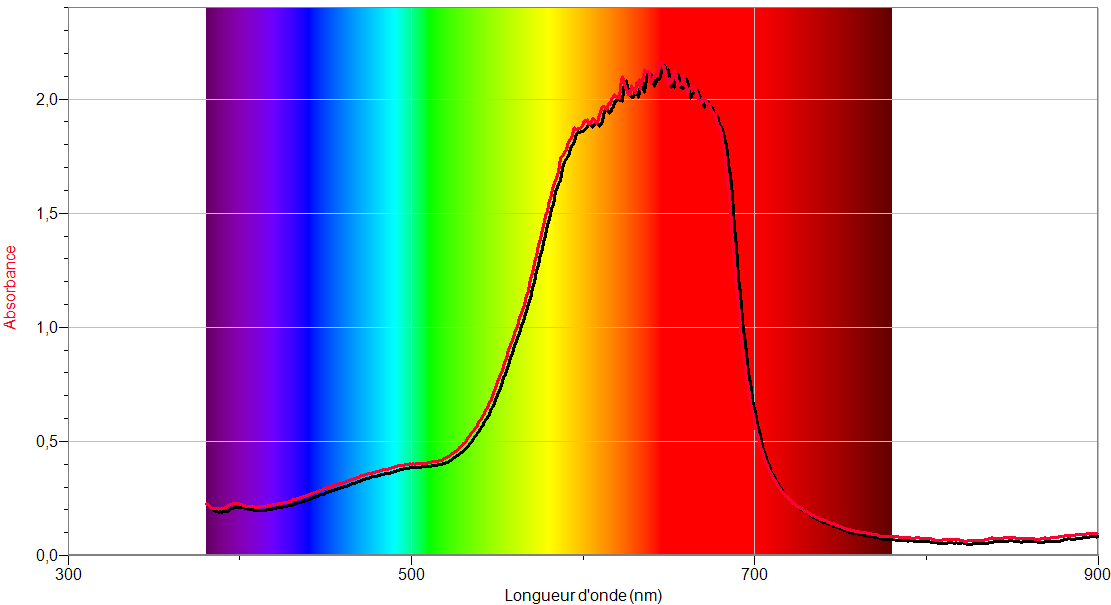
Encore une fois, afin de valider la pertinence des résultats, j'ai mesuré l'absorbance de la solution bleue avec mon spectrophotomètre Vernier.
Les résultats coïncident, avec un beau pic d'absorbance dans le rouge-orangé.
Étude de l'absorbance du colorant rouge
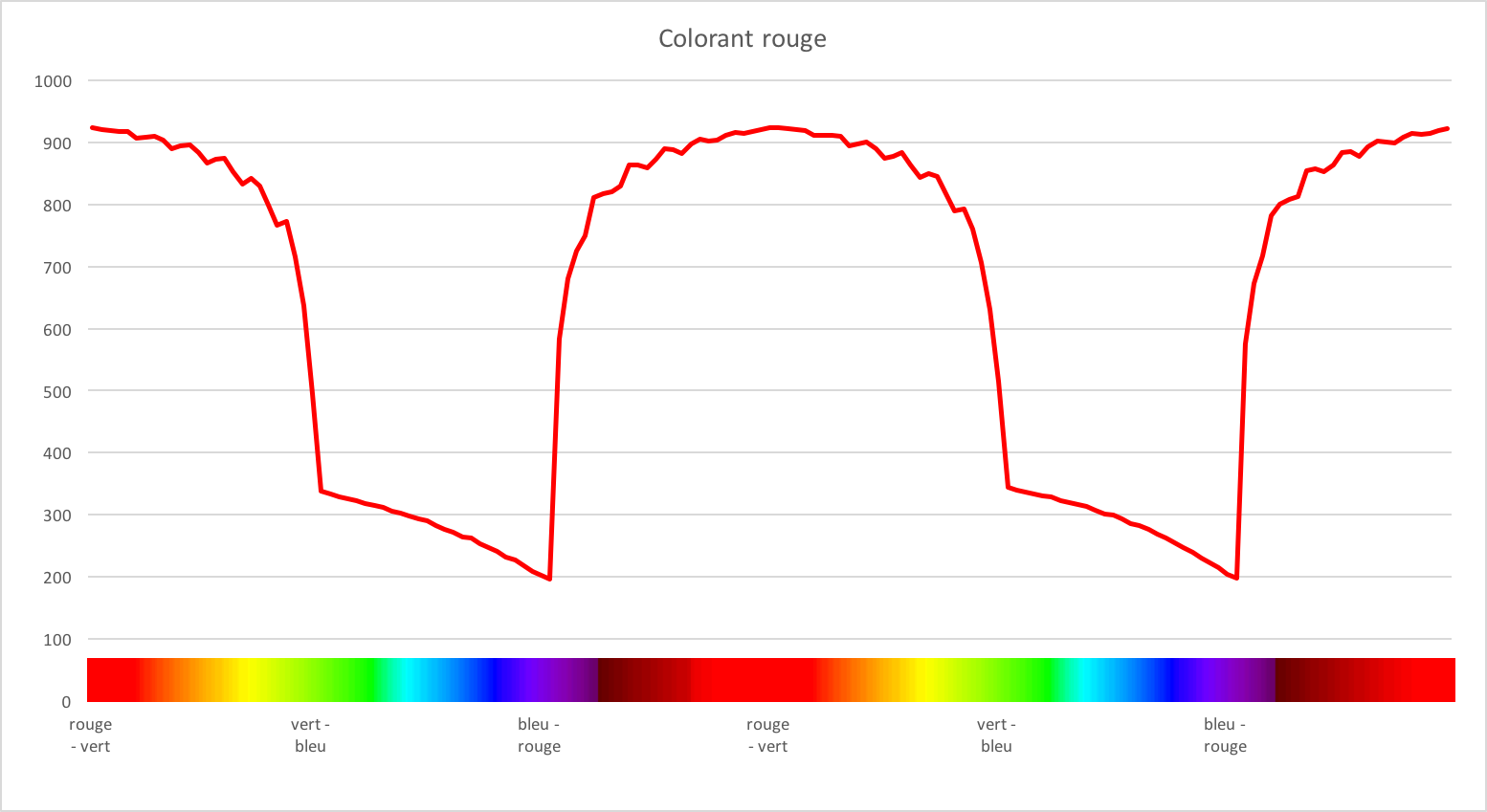
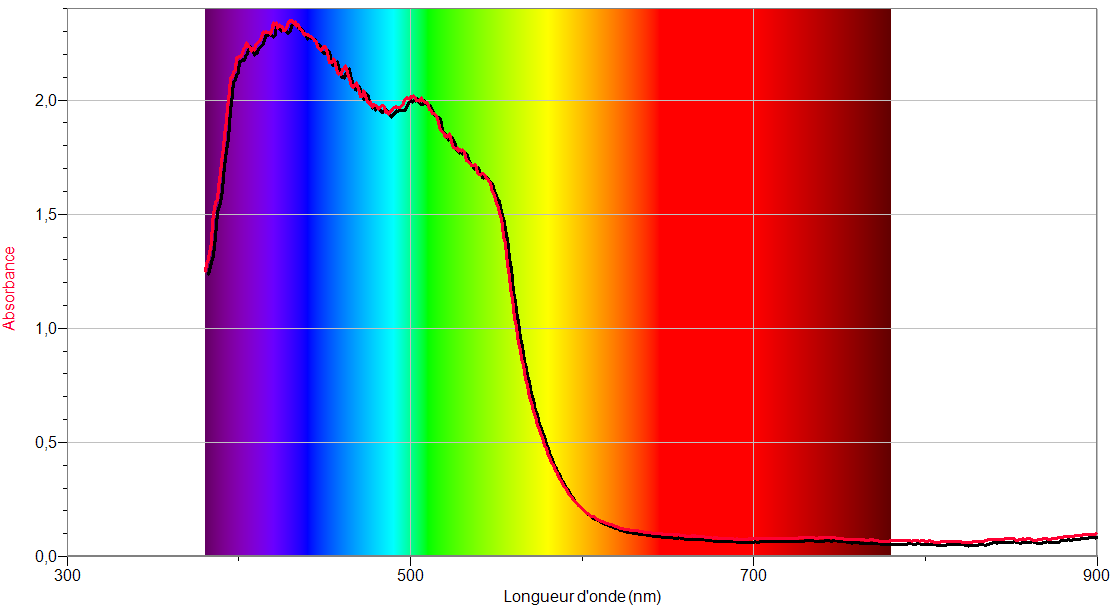
Nous observons un pic qui s'étale du vert au mauve, avec un maximum d'absorption dans le mauve. Notre colorant absorbe dans toutes les gammes correspondant au mauve-vert si l'on se réfère au cercle chromatique.
Et voici les données obtenues avec le spectrophotomètre Vernier.
Les résultats coïncident encore une fois, avec un beau pic d'absorbance étalé du mauve au vert.
Comparons les données pour les 3 colorants.
Étude comparée de l'absorbance des colorants rouge, vert et bleu.
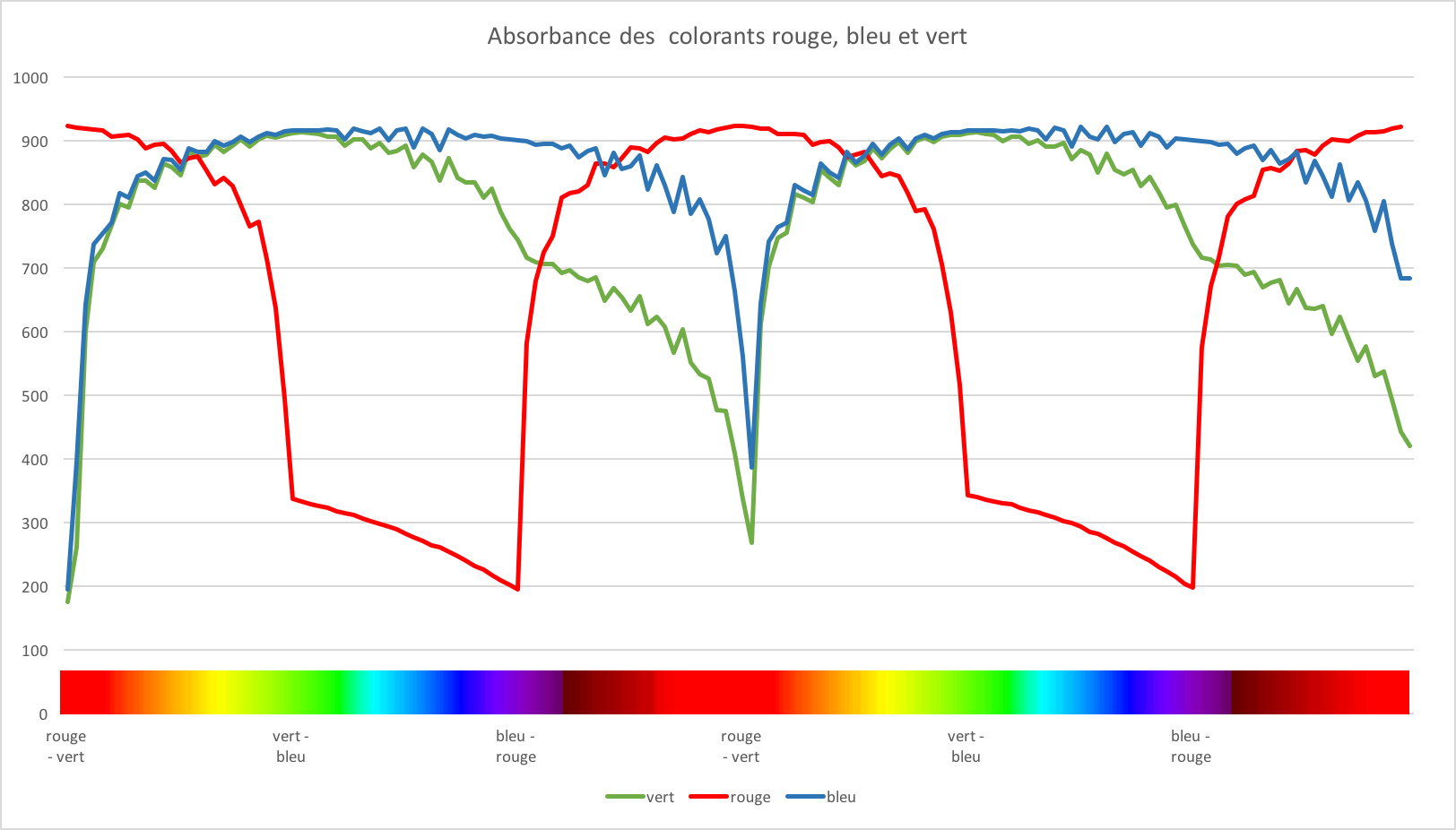
Nous constatons que chacune des solutions colorées a un profil d'absorption spécifique. Alors que le colorant bleu montre un pic d'absorption bien distinct dans le rouge orangé (environ 600-640 nm, voir figure), le vert et le rouge montrent un pic plus étalé. Le colorant vert absorbe principalement dans le rouge orangé (soit 640 nm environ) mais également le mauve (430 nm) alors que le rouge absorbe du mauve au vert, soit entre 430 et 530 nm.
Voici une première application de la spectrophotométrie. Il serait maintenant aisé de caractériser une couleur "à l'aveugle" par spectrophotométrie.
Imaginez maintenant que vous ayez un spectrophotomètre professionnel, bien plus sensible, et que vous vouliez mettre en evidence la présence d'un contaminant dans l'eau. Si vous connaissez la longueur d'onde lumineuse absorbée par ce contaminant, vous pourriez très rapidement mettre en évidence sa présence dans l'eau. Et au delà d'une analyse qualitative, la spectrophotométrie vous permettrait de doser la concentration de ce contaminant. C'est ce que nous allons voir dans la suite.
Comment doser une substance en solution par spectrophotométrie ?
Nous allons ici établir une courbe étalon mettant en relation la concentration d'une solutiom de bleu de méthylène et le signal obtenu au pic d'absorbance de la solution : la loi de Beer-Lambert-Bouguer.
Objectif
L'objectif est d'obtenir une relation directe entre absorbance et concentration d'une solution de bleu de méthylène. Une fois cette relation établie, nous pourrons nous servir de la courbe pour doser une solution de bleu de méthylène dont la concentration est inconnue.
Protocole expérimental
Il convient tout d'abord de préparer une solution mère de bleu de méthylène. Dans cette expérience, nous préparons une solution à 1% (1 mL de bleu de méthylène pour 100 mL d'eau distillée).
Nous effectuons ensuite des dilutions au 1/2 en cascade :
- 0,5% bleu de méthylène (dilution 1/2)
- 0,25% bleu de méthylène (dilution 1/4)
- 0,125% bleu de méthylène (dilution 1/8)
Nous allons également devoir mesurer l'absorbance d'une concentration nulle de bleu de méthylène. C'est le signal de base, un controle négatif, que l'on appelle également un blanc. Pour ce faire, préparez une cuve d'eau distillée.
Exécutez le programme et mesurez l'absorbance pour chacune des dilution, la solution mère et le blanc.
Compilez les données dans Excel et recueillez les valeurs du pic d'absorbance (les valeur les plus faibles). Comme il s'agit de la même teinte de bleu (plus ou moins pâle), les pics d'absorbance devraient avoir lieu dans tous les cas pour la même longueur d'onde (dans le rouge-orangé). Voici un exemple pour une dilution de bleu de méthylène. Recueillez la valeur exacte dans le tableau de données.
Résultats
Voici les spectrophotogrammes obtenus pour chacune des dilution de bleu de méthylène (C1, C2, C3) ainsi que la solution mère (C0) et le blanc.
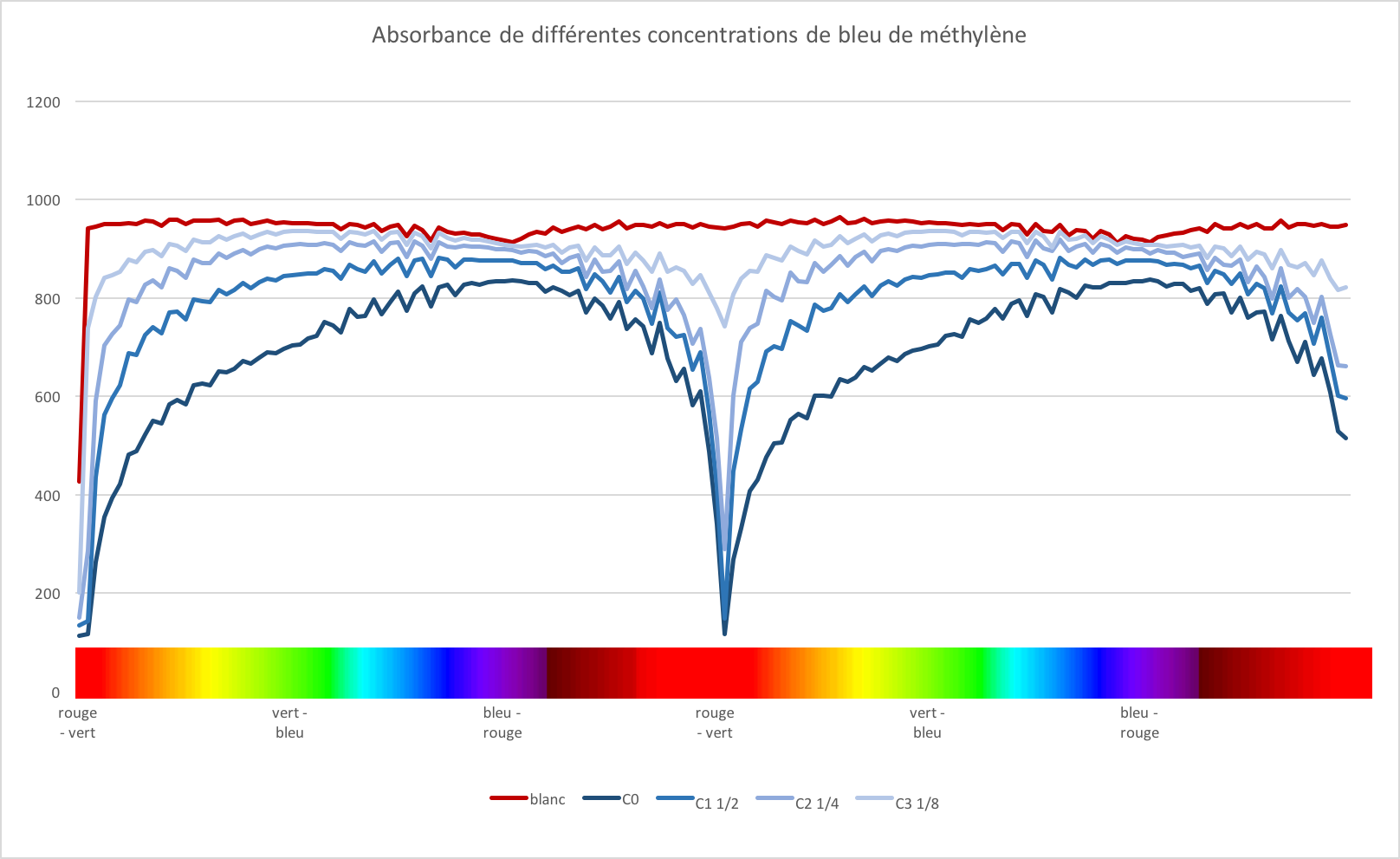
Constatez que plus la solution est concentrée, plus le pic d'absorption est bas : la solution absorbe de plus en plus si sa concentration augmente, il en résulte une plus faible lumière réfléchie et par conséquent un signal plus faible.
Le tableau suivant recense les valeurs des pics d'absorbance pour chaque dilution de bleu de méthylène
| Dilution de bleu de méthylène | Solution mère - 1% | Dilution 1/2 - 0,5% | Dilution 1/4 - 0,25% | Dilution 1/8 - 0,125% | Blanc- 0% (eau) |
|---|---|---|---|---|---|
| Signal obtenu lors du pic d'absorbance | 117 | 149 | 290 | 742 | 942 |
Représenté sous forme graphique, nous obtenons la courbe étalon suivante.
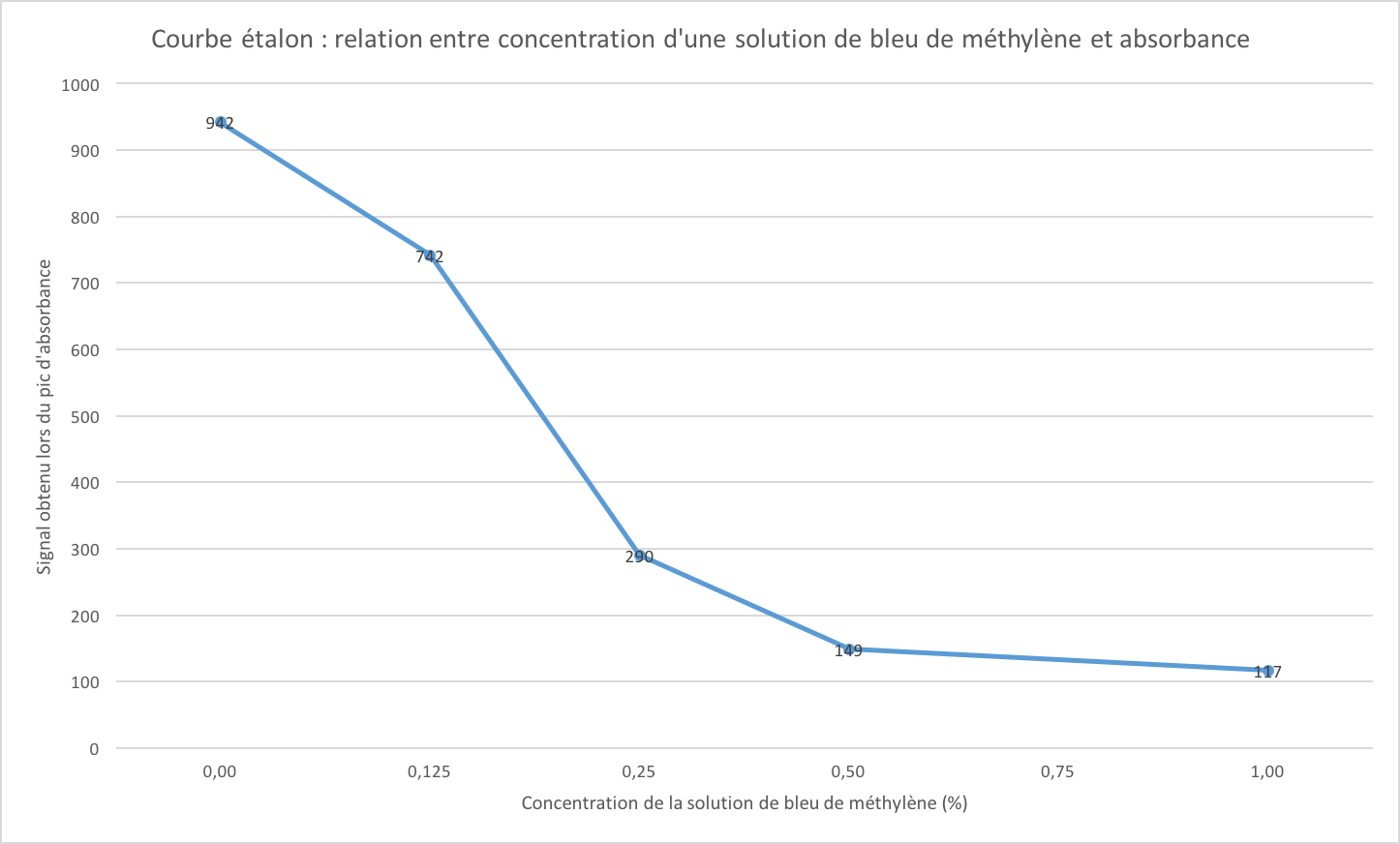
Grâce à cette courbe étalon, nous pourrions doser une solution de bleu de méthylène dont la concentration est inconnue. Il suffirait de mesurer son absorbance par spectrophotométrie et de voir à quelle concentration cela correspond en abscisses.
La spectrophotométrie n'a maintenant plus de secrets pour vous !
Il vous sera maintenant aisé de doser une solution de bleu de méthylène, dont la concentration est inconnue, par spectrophotométrie.
C'est quand même un projet sympa, relativement facile au vu de la complexité du sujet, et qui marche bien ! Arduino est un outil qui nous surprend toujours pour le potentiel qu'il offre, même dans sa plus simple expression comme c'est le cas dans cette activité. Une DEL, une photorésistance et nous voilà avec un systéme expérimental digne (ou presque !) des laboratoires de recherche !
Laissez un commentaire ci-dessous si vous avez aimé / pas aimé / compris / rien compris !






Voici une activité passionnante de physique optique expérimentale avec Arduino !
La spectrophotométrie est une méthode analytique qui permet de mesurer l'absorbance (ou densité optique) d'une substance en solution. L'absorbance est mesurée à l'aide d'un spectrophotomètre, qui consite en une source de lumière, un prisme afin de sélectionner une longueur d'onde lumineuse spécifique et un capteur photosensible (voir figure 1 ci-contre)
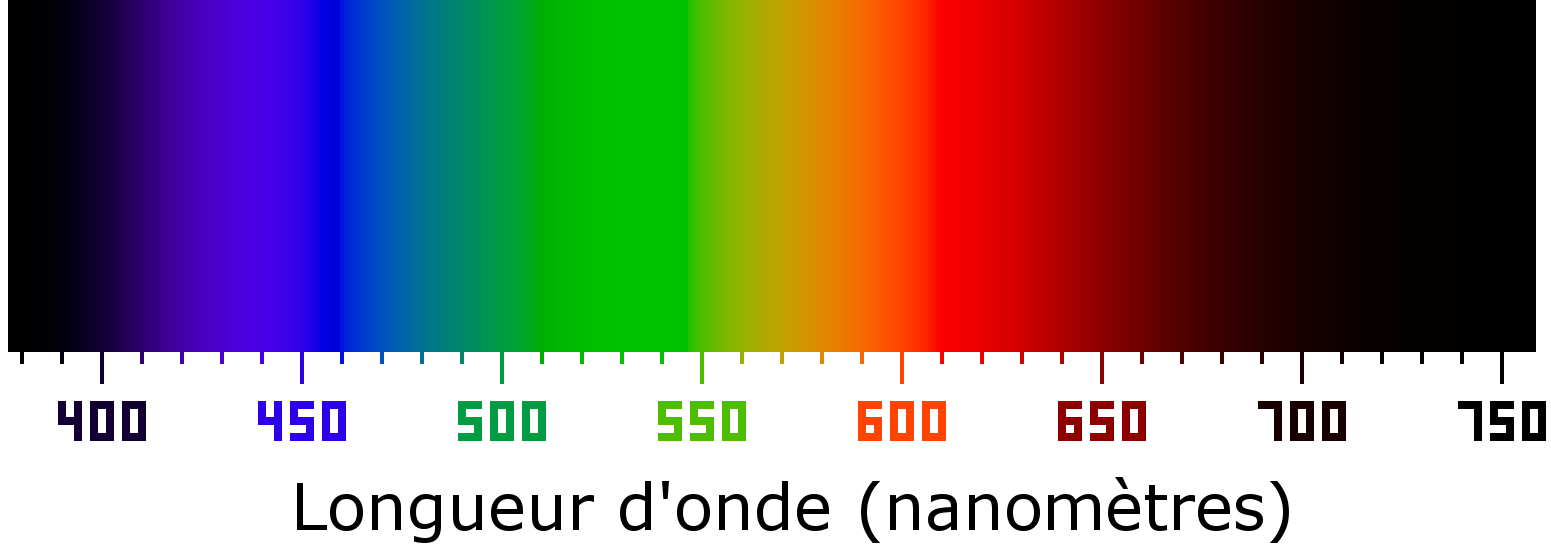
Concrètement, toute substance en solution est capable d'absorber certaines longueurs d'ondes lumineuses, que ce soit dans le spectre de la lumière visible ou invisible, des ultra-violets aux infra-rouges en passant par toutes les couleurs de l'arc-en-ciel (voir figure 2 ci-contre).
Par exemple, si vous voyez une pomme rouge, c'est parcequ'elle absorbe toutes les couleurs, principalement le vert et le bleu, sauf le rouge, entre 600 et 650 nanomètres (nm), qui nous est réfléchi et que l'on perçoit. On dit alors que la pomme abosorbe dans le vert et le bleu, soit entre 450 et 550 nm. Par conséquent, si cette pomme était éclairée avec une lumière émettant à 500 nm, elle nous paraîtrait noire ou grise. Si nous pouvions mesurer l'absorbance de cette pomme avec un spectrophotomètre, nous verrions lorsqu'on l'éclaire avec une longueur d'onde lumineuse de 550 nm un pic d'absorbance : la pomme absorbe la longueur d'onde émise et ne réfléchi rien. Dans un spectrophotomètre, la cellule photosensible ne recevrait plus de lumière, et nous verrions le signal diminuer fortement.